SOP(標準作業手順書)とは?
SOP(Standard Operating Procedure)は、日本語で「標準作業手順書」と訳され、特定の業務や作業を行う際の標準的な手順を文書化したものです。医療機器業界において、SOPは品質管理システム(QMS)の重要な要素の一つとして位置づけられています。
SOPに似通ったものとして「実施要領書」があります。これは、SOPに含まれる特定の作業、機器の操作方法などをまとめたもので、「作業手順書」、「ワークインストラクション」、「マニュアル」などと呼ばれることもあります。
具体的な定義
SOPとは、ある特定の業務や作業を行う際に、誰が、いつ、どこで、何を、どのように行うかを詳細に記述した文書のことを指します。これは、単なる作業マニュアルではなく、法令遵守や品質管理の観点から重要な役割を果たす品質文書です。
医療機器業界では、製品の設計、製造、検査、保管、出荷などの各工程において、SOPが作成され、厳密に管理されています。例えば、滅菌処理を行う医療機器の製造ラインでは、「滅菌工程SOP」といった具体的な手順書が存在し、滅菌の方法、時間、温度、確認方法などが詳細に記載されています。
目的
SOPの主な目的は以下の通りです:
- 品質の一貫性確保: SOPを通じて標準化された手順を実施することで、製品やサービスの品質を一定に保つことができます。医療機器の場合、患者の安全に直結するため、品質の一貫性は特に重要です。
- エラーの防止: 明確な手順を文書化することで、作業者の誤りや判断ミスを減らすことができます。例えば、複雑な組立工程を持つ医療機器の製造において、SOPは作業者が正確に手順を追うためのガイドラインとなります。
- 法令遵守の徹底: 医療機器業界は厳格な規制下にあり、SOPはこれらの規制要件を満たすための重要なツールとなります。例えば、PMDA(独立行政法人 医薬品医療機器総合機構)のQMS調査に備えて、製造プロセスの各段階でSOPを整備することが求められます。
- 知識の継承と教育: SOPは組織の知識や経験を文書化したものであり、新しい従業員の教育や技術の継承に役立ちます。例えば、ベテラン技術者の退職時に、その専門知識をSOPとして残すことで、組織の技術力を維持することができます。
- 継続的改善の基盤: SOPは定期的に見直され、改訂されることで、業務プロセスの継続的な改善につながります。例えば、新しい技術や規制の変更に合わせてSOPを更新することで、常に効率的で最適な手順を維持できます。
このように、SOPは医療機器業界において、高品質な製品を安定して提供し、患者の安全を確保するための重要なツールとして機能しています。
SOPの必要性
なぜ必要なのか?
医療機器業界においてSOPが必要とされる理由は多岐にわたりますが、主に以下の点が挙げられます:
- 患者の安全確保: 医療機器は人命に直接関わる製品であり、その品質と安全性の確保は最優先事項です。SOPを通じて標準化された手順を実施することで、製品の信頼性を高め、患者の安全を守ることができます。
- 規制要件の遵守: 医療機器業界は、PMDAやFDA(アメリカ食品医薬品局)などの規制当局による厳しい監督下にあります。SOPは、これらの規制要件を満たすための具体的な方法を示す重要な文書となります。
- 品質管理システム(QMS)の基盤: SOPは、ISO 13485やFDA 21 CFR Part 820などの品質管理システム規格の要求事項を満たすための重要な要素です。これらの規格では、プロセスの文書化と管理が求められており、SOPはその中心的な役割を果たします。
- トレーサビリティの確保: 医療機器の製造過程や使用状況を追跡できることは、問題発生時の原因究明や改善に不可欠です。SOPを通じて各プロセスを文書化することで、製品のライフサイクル全体にわたる製品の安全性に関するトレーサビリティを確保できます。
- リスク管理: 医療機器の開発や製造には様々なリスクが伴います。SOPを通じてリスク評価や管理の手順を明確化することで、潜在的な問題を事前に特定し、対策を講じることができます。
対象となる活動や範囲
SOPの対象となる活動や範囲は、医療機器のライフサイクル全体にわたります。具体的には以下のような領域が含まれます:
- 設計開発:
- 設計開発計画の策定
- 設計仕様の作成
- プロトタイプの開発
- 設計検証と妥当性確認
- 製造:
- 原材料の受入検査
- 製造工程の各ステップ
- 品質管理試験
- 包装と表示
- 品質保証:
- 最終製品の検査
- 不適合品の管理
- 是正措置と予防措置(CAPA)の実施
- 市販後管理:
- 文書管理:
- 教育訓練:
- 施設・設備管理:
- サプライチェーン管理:
これらの各領域において、具体的なSOPが作成され、組織全体で遵守されることで、医療機器の品質と安全性が確保されます。
導入によるメリット
SOPを適切に導入・運用することで、医療機器メーカーは以下のようなメリットを得ることができます:
- 品質の向上と安定化: 標準化された手順により、製品品質のばらつきが減少し、高品質な医療機器を安定して提供できるようになります。
- 効率性の向上: 明確な手順が文書化されることで、作業の無駄や重複が削減され、業務効率が向上します。例えば、新製品の開発期間の短縮や、製造ラインの生産性向上につながります。
- コンプライアンスの強化: 規制要件に準拠したSOPを整備することで、法的要求事項への適合が容易になり、法令遵守の水準が向上します。
- リスクの低減: 潜在的な問題を事前に特定し、対策を講じることで、製品の欠陥や回収のリスクを低減できます。
- 知識の蓄積と共有: ベストプラクティスをSOPとして文書化することで、組織の知識が蓄積され、効果的に共有されます。
- トレーニングの効率化: 新入社員や異動者のトレーニングが、SOPを基に体系的に行えるようになり、教育の質と効率が向上します。
- 有効性の維持: SOPの定期的な見直しと更新を通じて、業務プロセスの有効性の維持が促進されます。
- ブランド価値の向上: 高品質な製品と確立されたQMSにより、企業の信頼性とブランド価値が向上します。
これらのメリットにより、医療機器メーカーは競争力を強化し、持続可能な成長を実現することができます。SOPの導入は初期段階では時間と労力を要しますが、長期的には大きな価値をもたらす投資と言えるでしょう。
SOP活用の具体例
※本記事で紹介している具体例や数値は、説明のために作成したイメージであり、実在の企業を基にしたものではありません。
成功事例:ABC医療機器株式会社の人工呼吸器製造ライン
ABC医療機器株式会社は、高性能な人工呼吸器を製造する中堅メーカーです。同社は、品質管理の強化と生産効率の向上を目的として、人工呼吸器の製造ラインにおけるSOPの全面的な見直しと再構築を行いました。
具体的な取り組みは以下の通りです:
- SOPの詳細化と視覚化: 従来のテキストベースのSOPを、写真やフローチャートを多用した視覚的なものに改訂しました。例えば、複雑な組立工程では、各ステップの写真と注意点を併記し、作業者が直感的に理解できるようにしました。
- デジタル化の導入: 紙ベースのSOPをタブレット端末で閲覧できるシステムを導入しました。これにより、最新版のSOPへのアクセスが容易になり、改訂履歴の管理も効率化されました。
- トレーサビリティの強化: 各工程でのチェックポイントを明確化し、作業者がリアルタイムで記録を入力できるシステムを構築しました。これにより、製品ごとの製造履歴が詳細に追跡可能となりました。
- 定期的な見直しと改善: 毎年SOP検討会を開催し、現場の意見を積極的に取り入れてSOPを改善する仕組みを確立しました。
成功の結果:
- 製品の不良率が導入前と比べて40%減少しました。
- 製造ラインの生産性が15%向上しました。
- FDA査察において、品質管理システムが高く評価され、指摘事項がゼロとなりました。
- 従業員の満足度調査において、「作業手順の明確さ」に関する評価が20%向上しました。
この事例から、SOPを単なる文書としてではなく、現場の実態に即した実用的なツールとして活用することの重要性が分かります。また、継続的な改善と従業員の参加を促すことで、SOPの効果を最大化できることが示されています。
失敗事例:XYZ医療システムズの血糖測定器リコール問題
XYZ医療システムズは、糖尿病患者向けの血糖測定器を製造する大手メーカーです。同社は、新製品の開発と市場投入を急ぐあまり、SOPの整備と遵守が不十分な状態で生産を開始してしまいました。
問題の経緯:
- SOP作成の遅れ: SOPの更新が間に合わず、一部の作業では旧版のSOPに従って生産を開始しました。
- 教育訓練の不足: 新しい製造プロセスに関する従業員への教育にSOP教育を含めないまま、生産が開始されました。
- 品質管理プロセスの不備: 最終製品の検査SOPにおける検査基準が不明確で、特定の不具合を検出できない状態でした。
- 変更管理の失敗: 製造過程で発生した変更が、正式なSOPの改訂要否の検討を経ずに実施されていました。
問題の顕在化:
市場に出荷された製品の一部で、血糖値の誤表示が発生しました。患者が誤った血糖値に基づいてインスリン投与を行う危険性が指摘され、大規模なリコールが必要となりました。
失敗の影響:
- 約50万台の製品がリコール対象となり、交換費用だけで数十億円の損失が発生しました。
- 複数の患者から損害賠償訴訟が提起されました。
- 規制当局から厳重警告を受け、一時的に新製品の認可プロセスが停止されました。
- 企業イメージが大きく損なわれ、株価が30%以上下落しました。
- 市場シェアが大幅に低下し、競合他社に顧客を奪われる結果となりました。
この失敗事例から学べる教訓:
- SOPの重要性: 正しい作業が実施できるように明確でわかりやすい手順書を作成することが重要です。
- 従業員教育の徹底: SOPの内容を従業員に十分に理解させ、実践させるための教育訓練が重要です。
- 品質管理の継続的改善: 製品の特性に応じた適切な品質管理SOPを策定し、定期的に見直すことが必要です。
- 変更管理の厳格化: 新製品開発や製造プロセスの変更時には、必ずSOPを更新し、それに基づいた生産を行うことが不可欠です。製造プロセスの変更は、たとえ小さなものでも正式な変更管理プロセスを経て、SOPへの影響を評価する必要があります。
- リスク管理の強化: 潜在的なリスクを事前に特定し、SOPに反映させることで、重大な問題の発生を防ぐことができます。
この失敗事例は、医療機器業界においてSOPが単なる形式的な文書ではなく、患者の安全と企業の存続に直結する重要な要素であることを示しています。適切なSOPの策定と運用は、このような深刻な問題を未然に防ぐための重要な防御線となります。
SOPの導入方法
医療機器業界でSOPを効果的に導入・運用するためのわかりやすい始め方ガイドを以下に示します。
1. SOPの必要性の理解と経営層のコミットメント
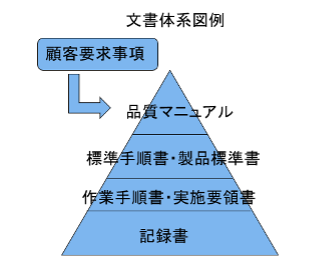
まず、組織全体で文書体系とSOPの位置づけ、SOPの重要性を理解し、経営層がその導入と運用にコミットすることが重要です。これにより、必要なリソースの確保や全社的な取り組みが可能になります。
2. 現状分析とギャップの特定
既存のプロセスを分析し、規制要件や業界標準との間にあるギャップを特定します。これにより、SOPが必要な領域や改善が必要な点が明確になります。
3. SOPの作成チームの編成
各部門の代表者や専門家で構成されるSOP作成チームを編成します。多様な視点を取り入れることで、実用的で効果的なSOPを作成できます。
4. SOPのテンプレートと形式の決定
組織全体で統一されたSOPのテンプレートと形式を決定します。一般的なSOPの構成要素には以下が含まれます:
- タイトルと文書番号
- 目的と適用範囲
- 関連文書
- 責任者と役割
- 用語の定義
- 手順の詳細(順序立てたステップ)
- 必要な記録と様式
- 改訂履歴
5. SOPの作成
特定された各プロセスについて、以下の手順でSOPを作成します:
a. プロセス、作業フローの詳細な分析 b. 手順のステップごとの記述 c. 関連する規制要件との整合性確認 d. 視覚的な要素(フローチャート、写真など)の追加 e. レビューと修正
6. SOPのレビューと承認
作成されたSOPは、関連部門の責任者や品質保証部門によってレビューされ、必要に応じて修正されます。最終的に、権限のある者(通常は上級管理職)による承認を得ます。
7. SOPの導入と教育訓練
承認されたSOPを関係者に周知し、適切な教育訓練を実施します。これには以下が含まれます:
8. SOPの運用と監視
SOPを実際の業務に適用し、その効果を監視します。定期的な内部監査やプロセスの観察を通じて、SOPの遵守状況と有効性を評価します。
このとき、SOPの承認から教育訓練の期間を得たうえで運用を開始する必要があることを考慮し、いつから運用を開始するかを明確にしておくことが重要です。
9. 見直し
法規制の変更、定期的なレビューや現場からのフィードバックに基づいて、SOPを適時に見直しします。一定期間、更新が行われていないSOPは、更新の必要がないかを定期的に確認し、常に最適な状態を維持します。
SOPの効果的な運用方法
SOPを効果的に運用するためには、単に文書を作成するだけでなく、組織全体でそれを活用し、継続的に改善していく必要があります。以下に、効果的な運用方法とその具体的な実践方法を説明します。
モニタリングと評価方法
- 定期的な内部監査:
- 頻度:少なくとも年1回、可能であれば半年に1回
- 方法:監査チェックリストを用いて、SOPの遵守状況を確認
- ポイント:単なる文書や記録等の書類確認ではなく、実際の作業観察、作業者へのインタビューも含める
- プロセス指標の設定と測定:
- 例:手順に関する不適合の発生率、作業の所要時間、SOPの理解度など
- 測定頻度:プロセスの重要度に応じて月次、四半期、半年ごとで設定
- 可視化:ダッシュボードやグラフを用いて、誰もが傾向を確認できるようにする
- 従業員フィードバックの収集:
- 方法:作業員へのアンケート、提案箱の設置など
- 頻度:随時
- 重要点:匿名性を確保し、率直な意見を集められるようにする
- トレーサビリティの確保:
- 記録作成日をSOPの版と紐付けて管理
- 電子記録システムの導入により、データの追跡と分析を容易に
- マネジメントレビュー:
- 頻度:年1回以上
- 内容:SOPの有効性、改善の必要性、リソースの適切性などを経営層で議論
よくある課題とその対応方法
- 課題:SOPが現場の実態と乖離している 対応:
- 定期的な現場観察を実施し、SOPと実際の作業の差異を特定
- 現場作業者を交えたSOP改訂ワークショップを開催
- 「仮SOPプロセス」を導入し、改訂案を試行的に運用して問題点を洗い出す
- 課題:SOPが複雑すぎて理解しにくい 対応:
- ビジュアル要素(フローチャート、写真、動画など)を積極的に活用
- 重要なポイントを強調表示し、チェックリスト形式を取り入れる
- 責任と役割を明確にする
- 難解な専門用語には定義を付け、用語集を作成する
- 課題:SOPの更新が追いついていない 対応:
- 定期的なSOPレビューサイクルを確立(例:年一回)
- 変更管理プロセスを強化し、プロセス変更時のSOP更新要否評価を必須化
- SOPの電子管理システムを導入し、更新と配布を効率化
- 課題:従業員のSOPに対する意識が低い 対応:
- SOPの重要性に関する定期的な教育セッションを実施
- SOPの遵守度を評価指標に組み込み、人事評価と連動させる
- SOPの改善提案制度を設け、積極的な参加を奨励する
- 課題:部門間でのSOPの整合性が取れていない 対応:
- クロスファンクショナルなSOP検討会を定期的に開催
- SOPの相互レビュープロセスを確立し、関連部門の承認を必須化
- 全社的なSOP管理システムを導入し、整合性チェックを自動化
- 課題:SOPの効果測定が適切に行われていない 対応:
- 各SOPに対応したKPI(重要業績評価指標)を設定
- データ分析ツールを活用し、SOPの遵守度と品質指標の相関を分析
- 定期的なSOPの有効性レビューを実施し、マネジメントレビューで経営陣に報告
これらの運用方法と課題への対応を適切に実施することで、SOPを単なる文書としてではなく、組織の品質と効率を継続的に向上させるツールとして活用することができます。重要なのは、SOPを固定的なものとしてではなく、常に進化し改善されるべきものとして捉えることです。そうすることで、医療機器業界の厳しい品質要求に応えつつ、組織の競争力を高めることができるでしょう。
まとめ
SOP(標準作業手順書)は、医療機器業界において品質管理と患者安全を確保するための重要なツールです。適切に策定・運用されたSOPは、一貫した製品品質の維持、法令遵守の徹底、業務効率の向上、そしてリスク低減に大きく貢献します。しかし、SOPの効果を最大化するためには、単に文書を作成するだけでなく、組織全体でその重要性を理解し、日々の業務に適切に組み込んでいく必要があります。
継続的な改善、従業員の積極的な参加、そして最新の規制要件や技術動向への対応を通じて、SOPを組織の強みへと転換することができます。医療機器業界の厳しい品質要求に応えつつ、イノベーションを推進するためにも、SOPの効果的な運用は不可欠です。今後も、デジタル化やAI技術の進展に合わせてSOPの在り方も進化していくことでしょう。組織の成長と患者の安全を両立させるための重要なツールとして、SOPの重要性は今後さらに高まっていくと考えられます。